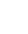痴呆模型
四川格林泰科依托成熟的动物实验平台和经验丰富的技术团队,可为全球客户提供系统、规范的痴呆动物模型构建及体内药效学评价服务,支持新药作用机制研究和非临床开发。
痴呆简介
痴呆是一类以获得性、进行性认知功能障碍为主要特征的中枢神经系统疾病综合征,主要表现为记忆力、学习能力、执行功能及社会行为等多方面功能的持续下降,严重影响患者的日常生活和社会功能。根据病因和病理机制的不同,痴呆可分为多种类型,包括神经退行性相关痴呆、血管性痴呆及代谢性疾病相关认知障碍等。在多种痴呆类型中,神经退行性改变是其共同的重要病理基础之一,主要特征包括神经元和突触丢失、神经网络结构破坏以及胶质细胞异常激活。从分子和细胞水平看,痴呆的发生发展通常与异常蛋白沉积、神经炎症反应增强、氧化应激失衡以及神经递质系统功能紊乱等多种机制相关。
阿尔茨海默症(Alzheimer's disease,AD)是痴呆中最常见的一种类型,其典型病理改变包括β-淀粉样蛋白(Aβ)异常沉积、Tau蛋白过度磷酸化、神经纤维缠结形成,以及随之发生的神经元和突触丢失。由于其病理特征明确、模型体系成熟,AD常被作为研究痴呆发生机制和药物干预策略的重要代表性疾病。
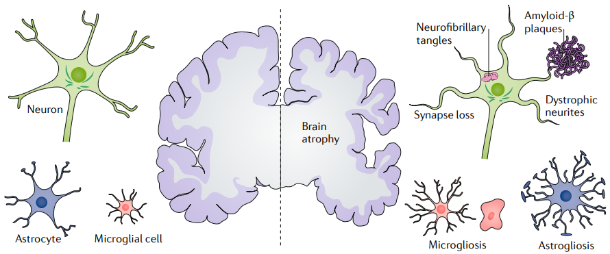
图1. 阿尔茨海默症的典型病理特征:脑萎缩、突触和神经元丢失、Aβ斑块、NTFs、营养不良的神经元突起、小胶质细胞和星形胶质细胞增生(Congdon & Sigurdsson 2018)。
除AD外,慢性脑低灌注、糖脂代谢异常等因素亦可引发认知功能损害,形成血管性痴呆或代谢相关认知障碍,其病理改变与神经退行性痴呆在一定程度上相互交叉。不同类型痴呆在病因、病理进程和干预靶点方面存在差异,因此,构建具有针对性的痴呆动物模型,是系统开展机制研究和药物非临床评价的关键基础。
可提供的痴呆模型
1、APP/PS1双转基因小鼠
转入人源β-淀粉样蛋白前体(APP)基因的小鼠表现出Aβ相关病理特征,引入PS1基因的APP/PS1双转基因小鼠相较于APP转基因小鼠,Aβ沉积和老年斑形成速度加快,学习记忆障碍显著提前,伴有神经元丢失、胶质增生和突触丢失等改变,是研究阿尔兹海默症的理想模型,导致早发型老年痴呆症。4月龄出现老年斑SP,6月龄出现Aβ沉积,10-12月龄出现记忆相关的行为学障碍。
应用:由于APP/PS1双转基因小鼠无法形成NFTs,适合用于靶向Aβ药物的非临床评价。
缺点:无神经退行性病变、脑萎缩和TNFs。
2、5xFAD小鼠
5xFAD小鼠,又被称为Tg-5xFAD小鼠,于2006年培育成功,包含了人类APP与PSEN1 2个基因位点上的5种突变。5xFAD小鼠具有明显的淀粉样蛋白病理改变特征,大约在2-4月龄时大脑出现斑块,伴有小胶质细胞增生、炎症反应,以及突触和神经元丢失。相较于APP/PS1小鼠,5xFAD小鼠疾病进展更快,已广泛应用于阿尔茨海默症疾病研究。
应用:5xFAD小鼠适用于探索与阿尔茨海默症相关的病理机制及免疫反应在神经退行性变中的作用,及相关药物临床前开发。
缺点:无NFTs形成。
3、SAMP8小鼠 – 自发型衰老模型
SAM小鼠(Senescence accelerated mouse)呈现出加速衰老的表型,包含一系列近交品系,可分为P系和R系,P系为快速老化小鼠(Senescence accelerated mouse/prone, SAMP),4-6月龄时出现反应迟缓、学习记忆功能障碍等老化特征;R系为抗快速老化小鼠,作为SAMP的正常对照。SAMP8亚系与正常小鼠相比,寿命更短、学习和记忆能力不足,在增龄过程中,APP表达水平显著升高,大脑中呈现出类似人类Aβ和Tau病理学特征,伴有氧化损伤、乙酰胆碱转移酶活力降低等人类AD相关病理特征。
应用:由于APP/PS1双转基因小鼠无法形成NFTs,适合用于靶向Aβ药物的非临床评价。
缺点:均一性较差、费用昂贵;很少出现Tau相关病理改变,不适合以Tau为药物靶点的新药研发。
4、糖尿病认知障碍模型
糖尿病可导致多种并发症,其中糖尿病认知障碍是中枢神经系统损害的常见表现之一。流行病学显示,2型糖尿病 (T2DM) 患者患阿尔茨海默症的发病率是没有T2DM人群的2.8倍。糖尿病认知障碍的病理生理学包括海马突触可塑性受损、神经营养因子水平降低、血脑屏障通透性增加、神经炎症升高和神经元凋亡增加等。
模型:格林泰科提供两种2型糖尿病认知障碍模型,包括db/db小鼠模型和High-Fat Diet (HFD)联合STZ诱导大鼠糖尿病模型。
5、2-VO血管性痴呆模型
血管性痴呆(Vascular dimentia, VD)是由于脑血管血流阻断或减少引发的大脑认知障碍。两血管阻断法(Two-vessel cclusion, 2-VO)是一款经典的血管性痴呆模型,可造成慢性脑低灌注状态和继发性白质损伤,被广泛用于探索血管性痴呆药物评价。2-VO血管性痴呆模型主要是通过结扎双侧颈总动脉实现,该模型操作简单,重复性好,成本低。
应用:2-VO大鼠血管性痴呆模型适用于研究血管性痴呆发病机制、病理改变、认知功能障碍,以及药效筛选评价。
6、东莨菪碱诱导模型 – 中枢胆碱系统损伤模型
东莨菪碱属于胆碱能拮抗药物,能穿过血脑屏障,抑制乙酰胆碱与受体结合,引发中枢胆碱系统紊乱,造成动物短期学习记忆障碍,可模拟AD患者行为的异常表现。向小鼠腹腔单次或多次注射东莨菪碱可引起脑内乙酰胆碱(ACh)水平显著下降,诱导AD动物模型。单次给药30min后即可出现明显学习记忆障碍,连续注射4周后,大鼠脑内Aβ和异常磷酸化Tau蛋白含量明显升高。
应用:适用于研究AD模型中的认知障碍和相关药物评价。
缺点:1、痴呆症状可逆;2、东莨菪碱对中枢M受体阻断为非特异性,动物可能出现焦虑、行动迟缓、自主活动增多等干扰行为学评价的不良反应。
动物种属:小鼠、大鼠
评价指标
1、神经行为学检测: Morris水迷宫实验(定位航行实验、空间探索实验)、避暗实验、新物体识别、巴恩斯迷宫、社交箱、旷场、转棒仪、高架十字迷宫等;
2、Aβ检测:1)ELISA检测Aβ含量(组织匀浆、血浆、脑脊液);2)老年斑组织染色(免疫组化);
3、Tau蛋白检测:WB法测定脑内过磷酸化Tau蛋白水平;
4、病理免疫组化:1)神经元数量;2)小胶质细胞数量;3)星形胶质细胞数量;4)NFTs;
5、大脑海马和皮层中AChE、ChAT活性及ACh含量测定,ELISA(东莨菪碱诱导模型);
6、神经炎症检测;
7、氧化应激检测。
案例展示
1、阿兹海默症APP/PS1双转基因小鼠模型
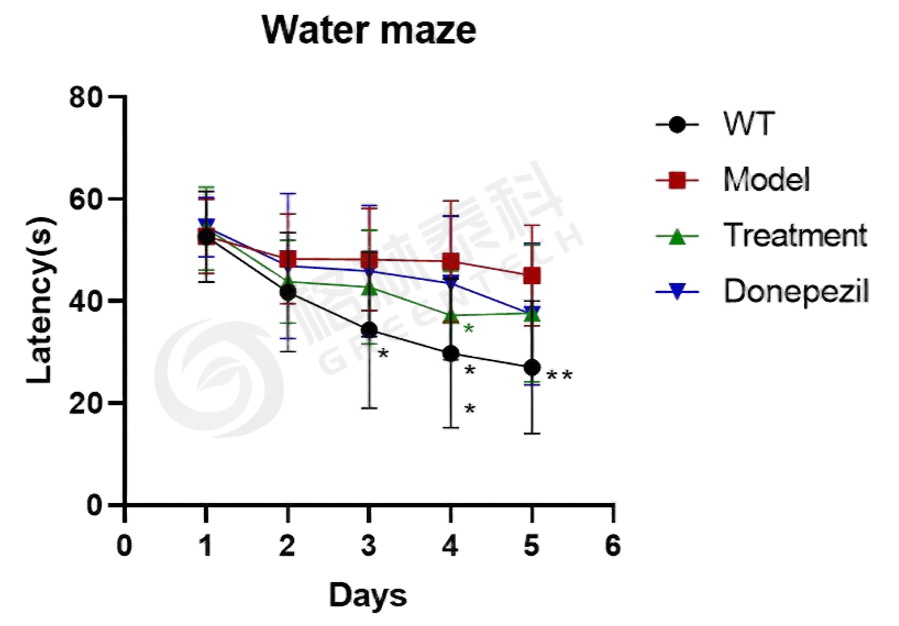
图2. APP/PS1双转基因小鼠模型-水迷宫实验。
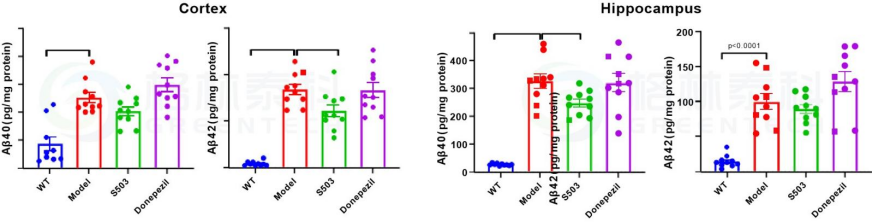
图3 APP/PS1小鼠大脑皮层和海马Aβ40和Aβ42含量
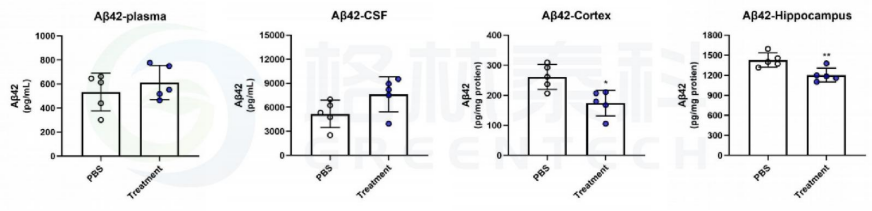
图 4. APP/PS1小鼠血浆、脑脊液、皮质、海马体Aβ42含量
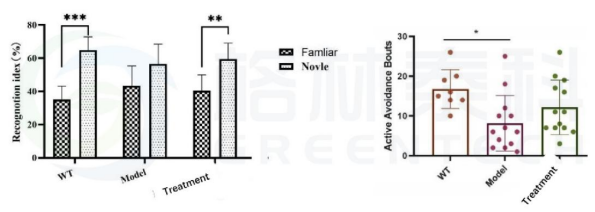
图 5. APP/PS1小鼠行为学检测-新物体识别和穿梭箱
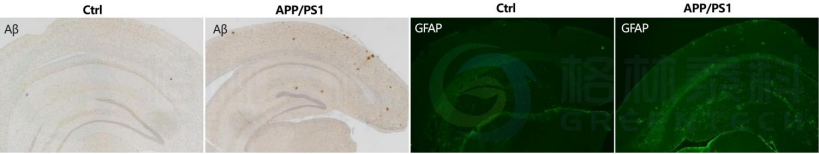
图 6. APP/PS1小鼠组织病理学检测-Aβ和GFAP染色
2、5×FAD小鼠神经功能衰退
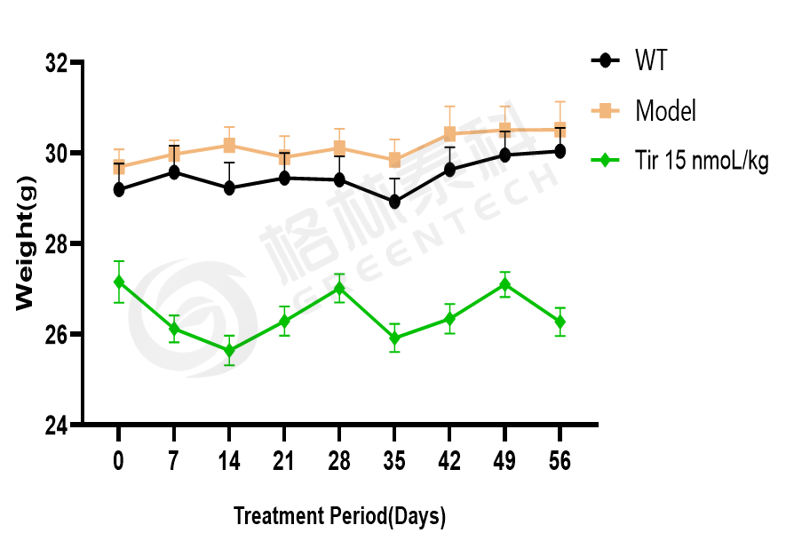
图7. 5×FAD小鼠体重变化
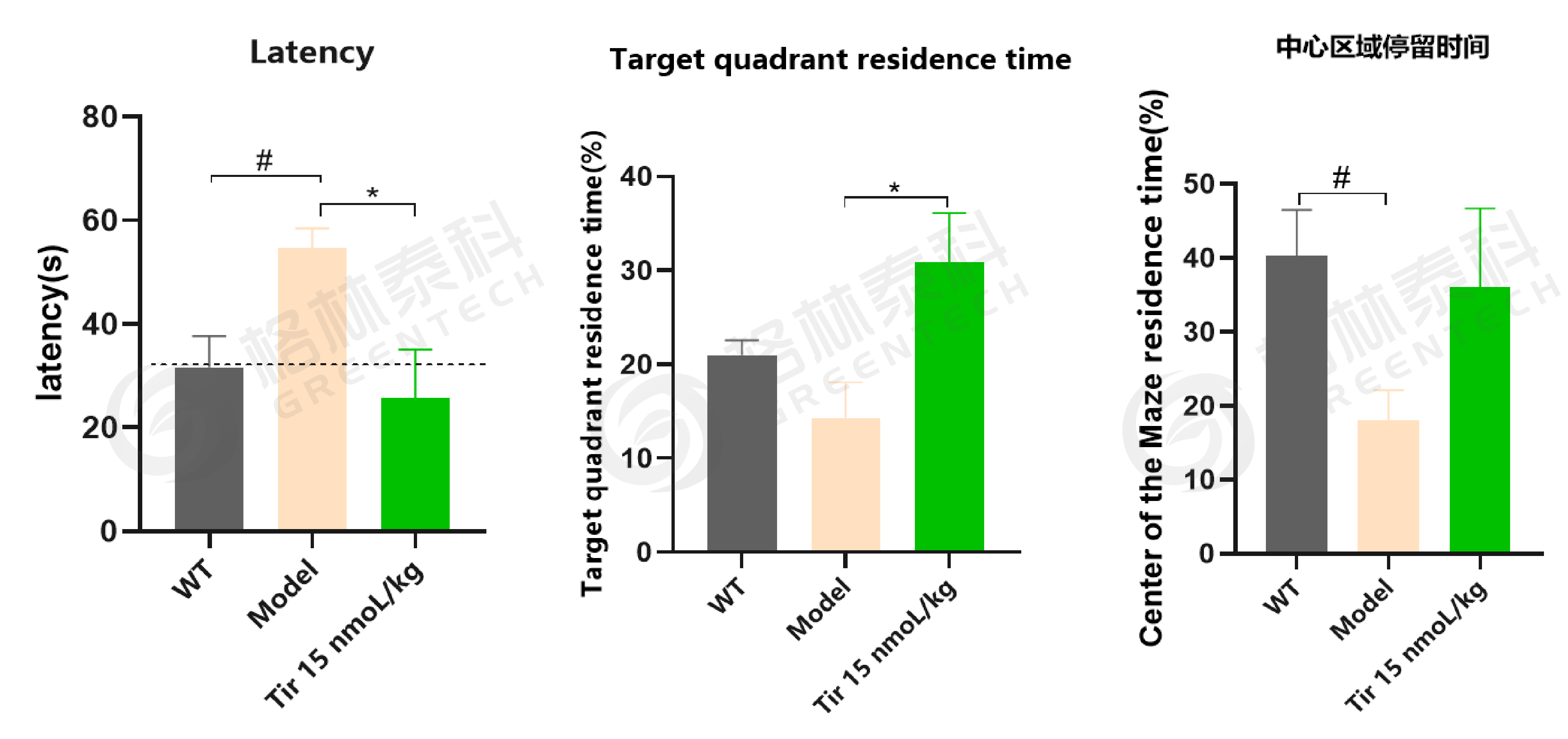
图8. 给药9周后 5×FAD小鼠模型水迷宫实验结果
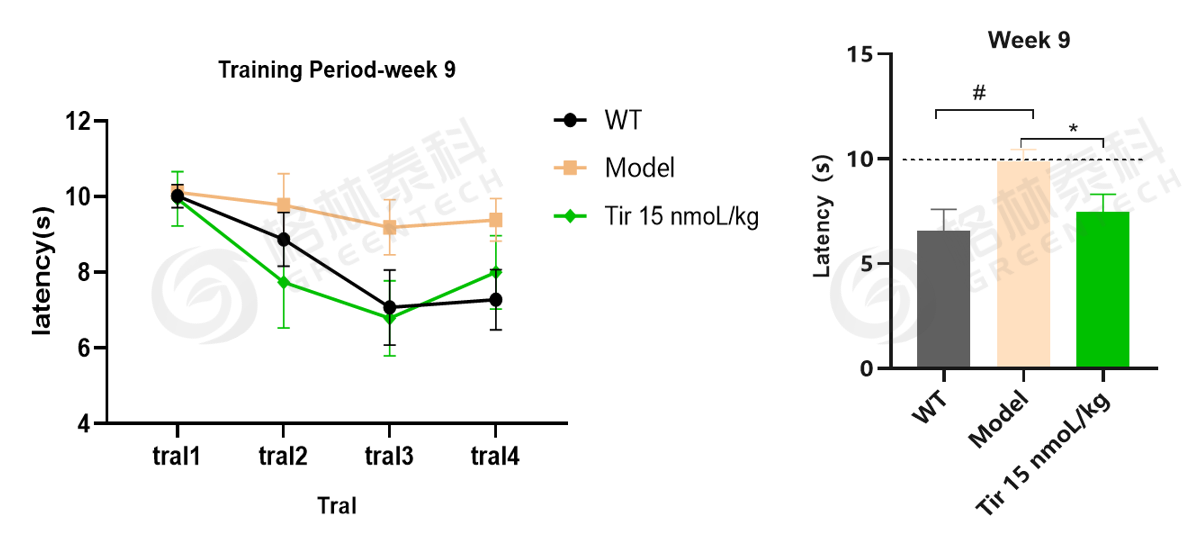
图9. 给药9周后5×FAD小鼠模型穿梭箱实验结果
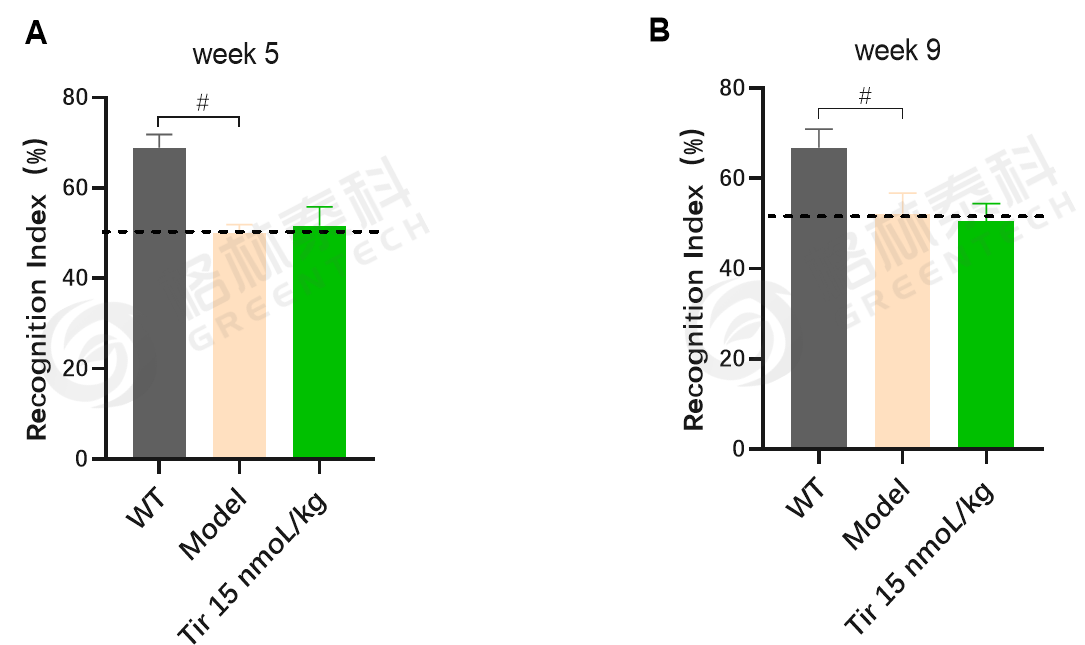
图10. 5×FAD小鼠模型新物体识别实验结果。
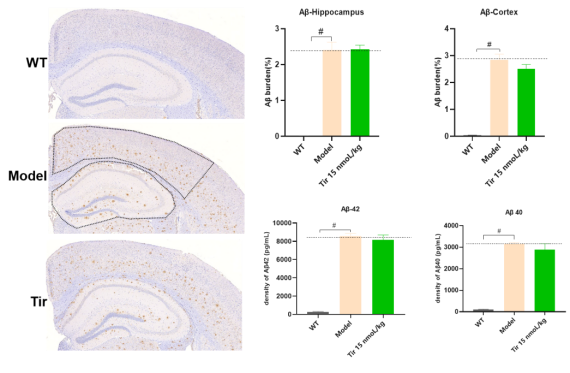
图11. 5×FAD小鼠模型脑组织Aβ染色结果。
欢迎随时联系我们,共同探讨您的高血压新药研发项目,体验我们的专业服务。
参考文献
1. Congdon E E, Sigurdsson E M. Tau-targeting therapies for Alzheimer disease[J]. Nature Reviews Neurology, 2018, 14(7): 399-415.
2. Götz J, Bodea L G, Goedert M. Rodent models for Alzheimer disease[J]. Nature Reviews Neuroscience, 2018, 19(10): 583-598.
3. Canudas AM, Gutierrez-Cuesta J, Rodríguez MI, et al. Hyperphosphorylation of microtubule-associated protein tau in senescence-accelerated mouse (SAM). Mech Ageing Dev. 2005;126(12):1300-1304.
4. Porquet D, Andrés-Benito P, Griñán-Ferré C, et al. Amyloid and tau pathology of familial Alzheimer's disease APP/PS1 mouse model in a senescence phenotype background (SAMP8). Age (Dordr). 2015;37(1):9747.
5. Das TK, Jana P, Chakrabarti SK, Abdul Hamid MRW. Curcumin Downregulates GSK3 and Cdk5 in Scopolamine-Induced Alzheimer's Disease Rats Abrogating Aβ40/42 and Tau Hyperphosphorylation. J Alzheimers Dis Rep. 2019;3(1):257-267.
6. 黄龙舰, 赵春阳, 冯新红,等. 抗阿尔茨海默病药物非临床药效学评价体系的探索[J]. 药学学报, 2020, v.55(05):35-51.
7. Forner S, et al. Systematic phenotyping and characterization of the 5xFAD mouse model of Alzheimer's disease. Sci Data. 2021 Oct 15;8(1):270. doi: 10.1038/s41597-021-01054-y. PMID: 34654824; PMCID: PMC8519958.
8. Ruan S, et al. Aerobic exercise alleviates cognitive impairment in T2DM mice through gut microbiota. Sci Rep. 2025 Jul 4;15(1):23917. doi: 10.1038/s41598-025-07220-1. PMID: 40615512; PMCID: PMC12227742.